近日,上海市重大传染病和生物安全研究院/上海市公共卫生临床中心范小勇/胡志东团队关于靶向结核潜伏感染的新型病毒载体疫苗研发取得突破进展,通过小鼠急性感染模型和潜伏感染模型分别证实了其抗结核感染和发病的免疫保护效力。该研究论文发表于Emerging Microbes & Infections期刊(中科院传染病学一区,IF=13.2)。

据世界卫生组织(WHO)报道,全球范围内约四分之一人口潜伏感染结核分枝杆菌。结核潜伏感染(LTBI)人群在其一生中,约十分之一人会发病并进展为活动性结核病。2018年的一项临床队列研究表明,LTBI人群每年罹患活动性结核病的概率为未感染人群的8.8倍。2019年,WHO发布的全球结核病研究报告认为,针对LTBI人群的免疫干预/治疗可更有效降低结核病传播及其疫情。因此,针对LTBI人群的暴露后预防性疫苗将能够针对潜在的疾病目标人群进行精准干预并有效控制结核病的发生和传播。
范小勇/胡志东团队前期在国际上首次使用仙台病毒作为结核疫苗载体构建了一株包含结核菌急性感染期免疫优势抗原的新型结核疫苗SeV85AB,通过动物实验证实了该病毒载体结核疫苗通过诱导肺组织定居记忆性T细胞而介导有效的抗结核保护作用。基于该研究基础,研究团队进一步进行了疫苗的改良,使其能够同时用于卡介苗接种人群的加强免疫及LTBI人群的暴露后预防,从而达到最优的免疫保护效果。
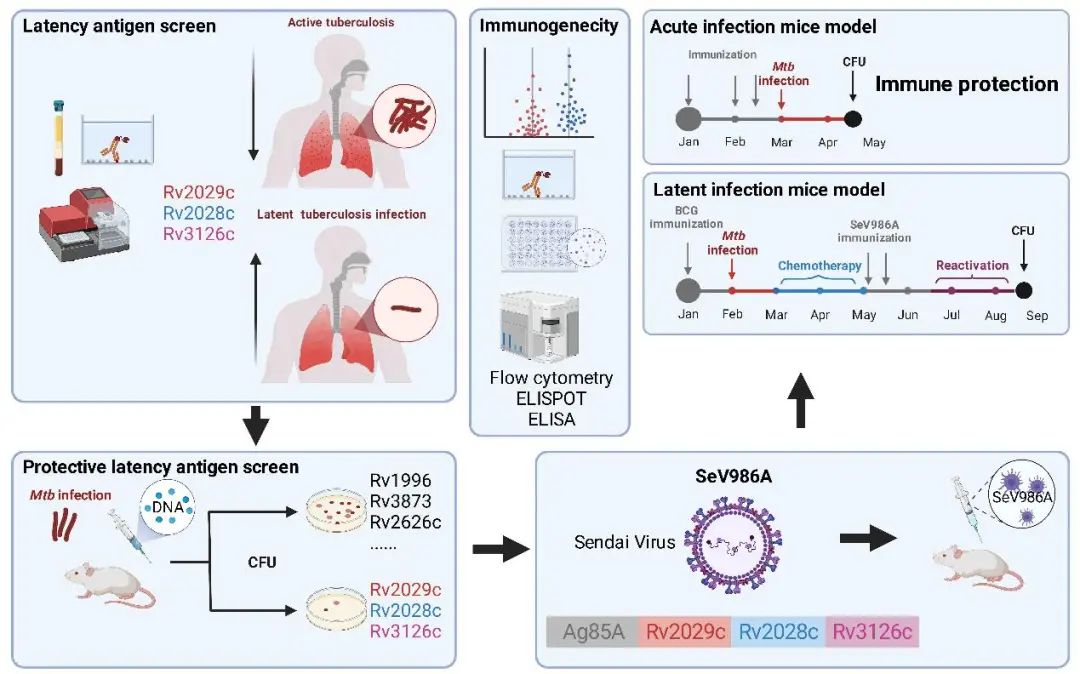
研究显示,潜伏性结核感染相关基因的表达与机体免疫保护正相关,即LTBI人群针对这些基因能产生抗原特异性应答,有助于该人群控制结核菌的复制而避免结核病的发生。
研究团队首先通过170人的研究队列,筛选出9个在LTBI人群中应答上调的抗原;然后,构建了这些抗原的重组DNA疫苗,通过小鼠结核感染模型分析其介导的免疫保护效力,成功筛选得到3个保护性抗原。最后,利用仙台病毒载体构建融合表达这3个潜伏感染抗原和急性期抗原Ag85A的新一代重组仙台病毒载体结核疫苗SeV986A。动物实验结果显示,该疫苗能有效诱导抗原特异性Th1型CD4 T和CD8 T细胞免疫应答及一定水平的抗体反应,进一步的动物保护试验则证实了该多抗原重组病毒载体疫苗在小鼠急性感染和潜伏感染模型中均能显著降低感染动物肺脏和脾脏的结核菌荷菌量以及肺脏的病理损伤,且在潜伏感染模型中保护力的提升与其抗原特异性T细胞耗竭的降低相关。因此,这种同时包含结核菌潜伏感染抗原与急性期抗原的抗原组合为结核病新疫苗的开发提供了有力的实验证据与新思路,所开发的多抗原重组仙台病毒载体疫苗亦有望在今后成为一种新型暴露后预防性疫苗并针对结核潜伏人群进行精准干预并有效控制结核病的发生和传播。

上海市重大传染病和生物安全研究院/上海市公共卫生临床中心范小勇研究员与上海市公共卫生临床中心胡志东副研究员为本文通讯作者,胡志东博士与复旦大学博士生夏静娴为第一作者。本项目得到了国家重点研发项目、国家自然科学基金、上海市优秀学术带头人和上海市卫生健康学术带头人等项目的支持。

