包括新型冠状病毒在内的冠状病毒感染在过去二十年严重影响了世界人民的身体健康、经济发展和社会稳定。除了三种高致病性的冠状病毒(SARS-CoV、SARS-CoV-2和MERS-CoV),普通冠状病毒(HCoV-OC43,HCoV-229E,HCoV-NL63,HCoV-HKU1)感染机体也会导致呼吸道疾病。然而,目前广谱抗冠状病毒药物和疫苗较为缺乏。针对这一关键科学问题,近期复旦大学基础医学院医学分子病毒学教育部/卫健委/医科院重点实验室、上海市重大传染病和生物安全研究院姜世勃/陆路团队在国际知名期刊Emerging Microbes & Infection(EMI, IF=13.2)以Research Article形式发表的研究论文。

新冠病毒S蛋白由S1和S2两个亚基组成,S2亚基含有fusion peptide (FP), heptad repeat 1 (HR1), central helix (CH), connector domain (CD), stem helix (SH), heptad repeat 2 (HR2)和transmembrane anchor (TM)等功能域。在病毒入侵靶宿主细胞时,S2亚基构象发生改变, HR1和HR2相互作用形成六聚体融合核心结构(6-HB),介导病毒膜和细胞膜的融合,是病毒入侵和感染宿主靶细胞的关键步骤之一。在S蛋白融合前构象中,S2亚基被S1亚基包裹,因此相对于含有RBD区的S1亚基更保守。一些研究发现靶向SH区的中和抗体对β属冠状病毒具有广谱中和作用。根据晶体结构分析,SARS-CoV-2 S2蛋白融合后构象中,HR1区和CH区形成长的中间三螺旋结构,SH区靠近CH区。因此,本研究以S2亚基的HR1、CH和SH三个功能区为基础设计了重组蛋白HR1、HR1S和HR1LS(图1)。
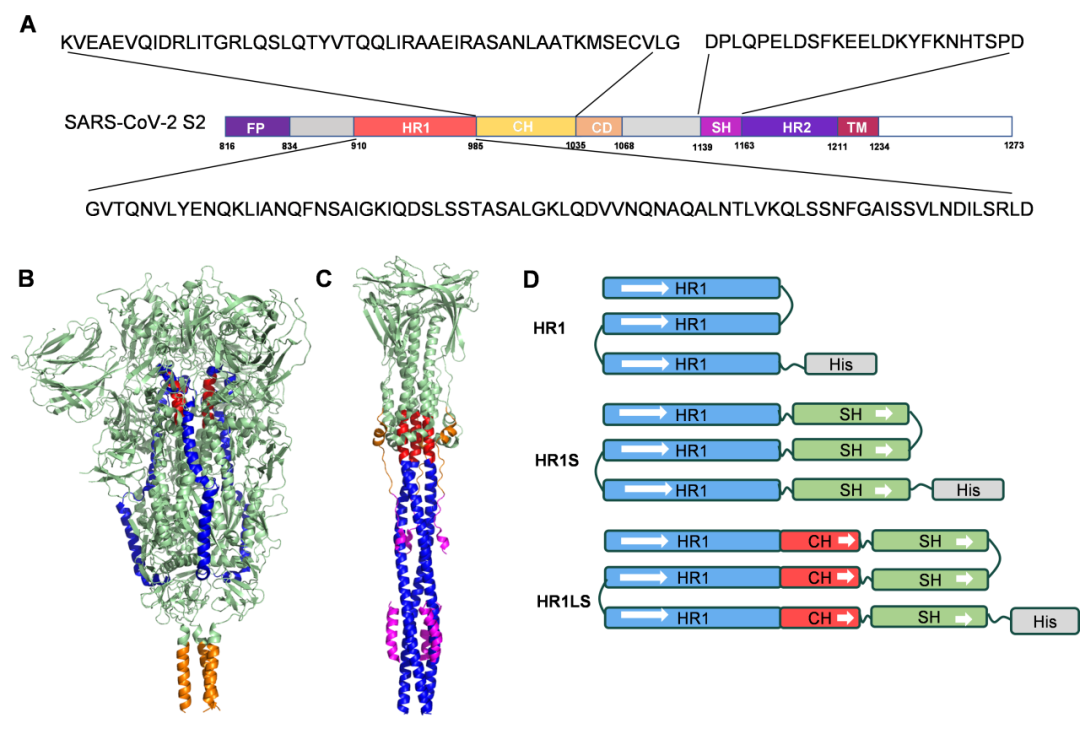
图1. SARS-CoV-2 S2亚基的模式图和三聚体蛋白的设计。(A)SARS-CoV-2 S2 亚基和HR1、CH和SH的氨基酸序列。(B) SARS-CoV-2 S蛋白的融合前构象中HR1(蓝色)、CH(红色)、SH (橙色)的位置和结构。(C) SARS-CoV-2 S2亚基在融合后构象,融合后状态下的HR2(粉红色)。(D)HR1、HR1S、HR1LS三聚体蛋白。白色箭头表示从N到C端的氨基酸序列。
利用Alphafold2预测发现三个重组蛋白能形成三聚体,具有典型的α螺旋结构,并且均能与SARS-CoV-2 HR2多肽(HR2P)结合(图2)。
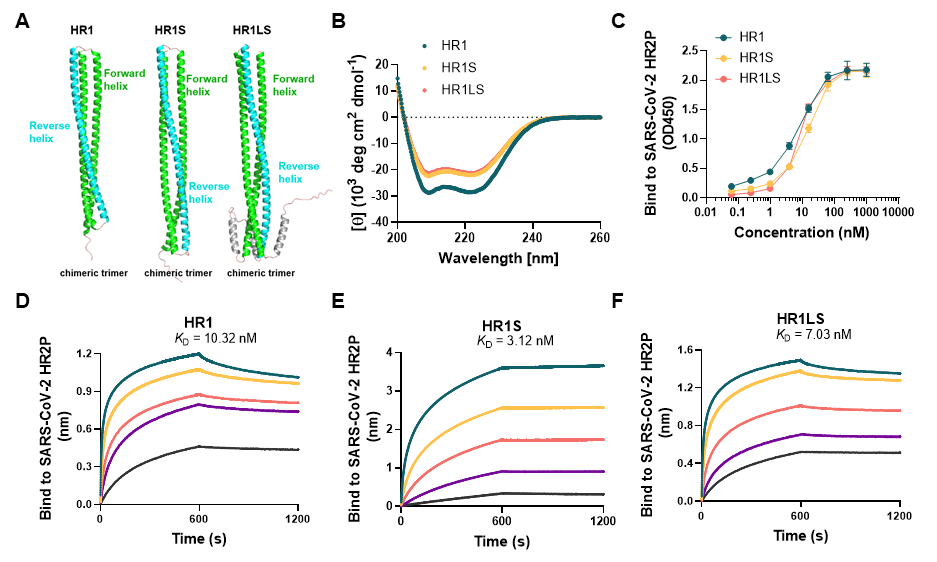
图2. HR1、HR1S和HR1LS的三维和二维结构分析及其与HR2P结合的亲和力
三聚体蛋白HR1、HR1S和HR1LS对SARS-CoV-2假病毒感染展现出高效抑制活性,其中HR1LS抑制活性最佳(图3)。HR1LS对Delta突变株、Omicron突变株(如BA.2.75、BQ.1、XBB和CH1.1)假病毒感染也显示出高效的抑制活性。最重要的是,HR1LS对SARS-CoV、MERS-CoV、HCoV- 229E、HCoV-NL63和MjHKU4r-CoV-1假病毒同样具有很好的抑制作用。
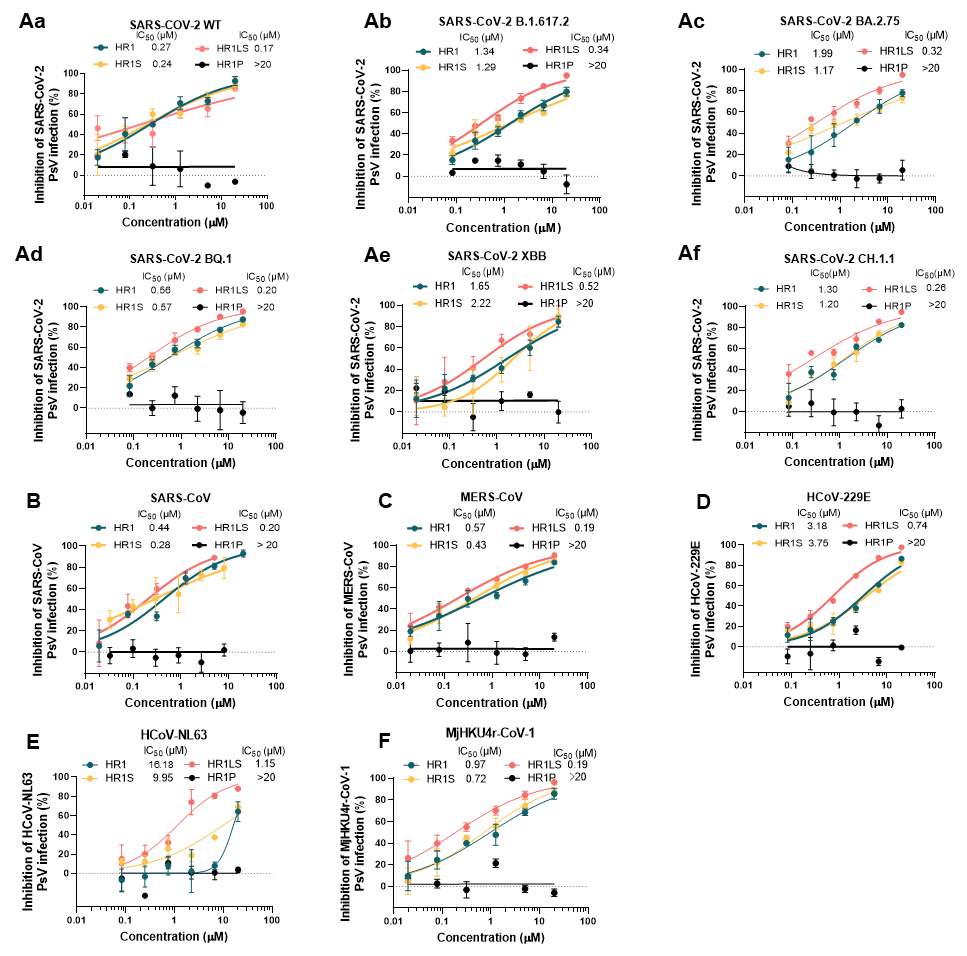
图3. HR1、HR1S和HR1LS对冠状病毒假病毒的抑制活性
进一步,该研究评估了HR1LS对活病毒及在动物体内的保护效果(图4)。结果显示HR1LS在体外能有效抑制HCoV-OC43活病毒感染。将HR1LS分别按10mg/kg和25mg/kg两个剂量,通过滴鼻途径给予乳鼠。无论是在攻毒前30 min单次给药,还是感染后三天连续给药3次,给药组乳鼠肺组织病毒载量较PBS组均下降,提示HR1LS对HCoV-OC43体内活病毒感染具有预防和治疗作用。
上述结果提示三聚体蛋白HR1LS具有广谱、高效抗冠状病毒感染的效力,可进一步地开发成通用冠状病毒(Pan-CoV)抑制剂药物,用来治疗和预防冠状病毒感染。
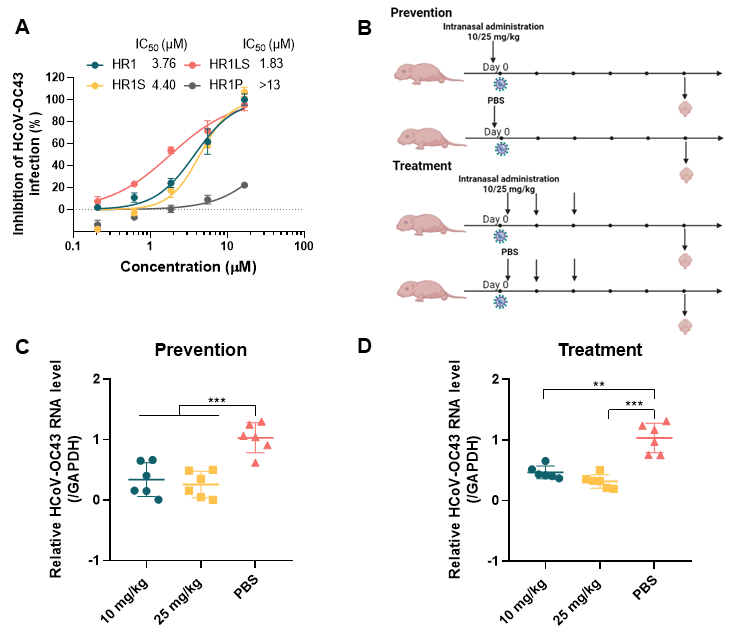
图4. HR1、HR1S和HR1LS对HCoV-OC43感染乳鼠的体内保护作用
本研究同时使用三种重组蛋白HR1、HR1S和HR1LS作为免疫原分别免疫小鼠。当与铝佐剂共同免疫时,HR1、HR1S和HR1LS均能诱导小鼠产生特异性抗体,而且小鼠血清能有效中和SARS-CoV-2假病毒感染。与HR1相比,HR1S和HR1LS还可诱导小鼠产生针对SH的抗体。其中HR1LS免疫小鼠血清中和SARS-CoV-2假病毒的抗体滴度最高,提示HR1LS具有更好的免疫原性。
由于该团队前期发现CF501佐剂与RBD-Fc共同免疫能激发强效的广谱中和抗体和T细胞免疫反应,他们进一步探究了重组蛋白HR1LS与CF501佐剂共同免疫小鼠的效果(图5)。结果表明三次免疫后,与HR1LS/Alum相比,HR1LS/CF501免疫后能诱导小鼠产生更高水平的SARS-CoV-2中和抗体。而在完成HR1LS/CF501第四次和第五次免疫后,小鼠血清中和SARS-CoV-2假病毒的抗体滴度是HR1LS/Alum组的3倍和4.4倍。
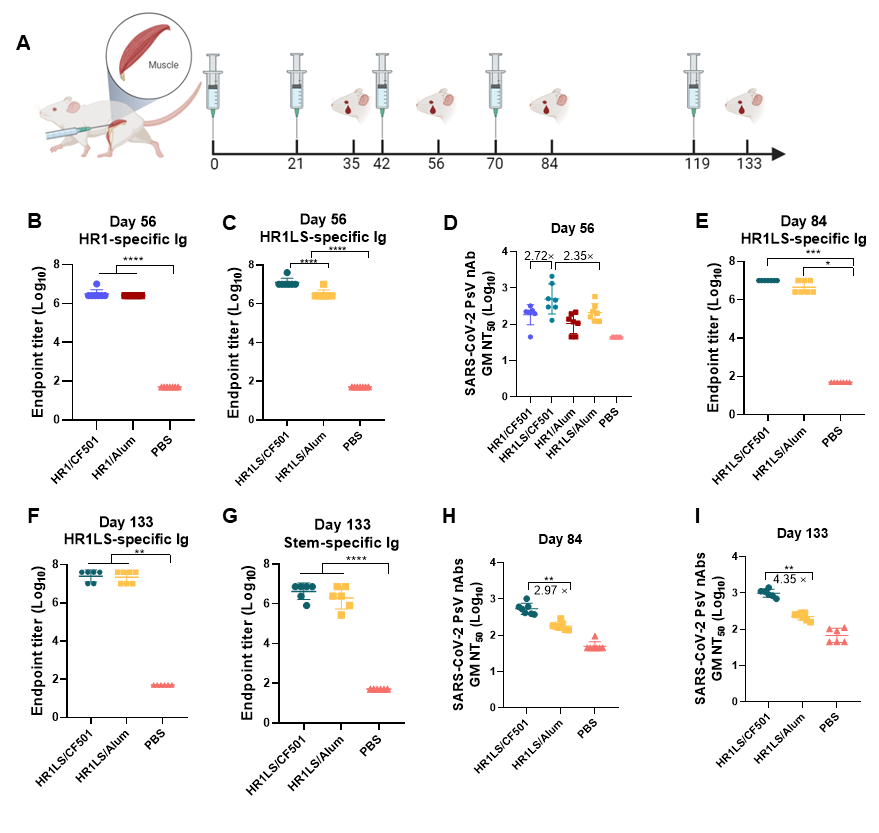
图5. HR1LS/CF501免疫小鼠诱导较强的结合和中和抗体反应
本研究也检测HR1LS/CF501免疫后小鼠血清对其他冠状病毒假病毒的中和效果(图6)。结果显示免疫后小鼠血清不仅对属于β-CoV的MERS-CoV和HCoV-OC43具有中和作用,而且对属于α-CoV的HCoV-229E和 HCoV-NL63也具有中和作用。更关键的是,免疫后小鼠血清对新发现的蝙蝠冠状病毒MjHKU4r-CoV-1同样具有中和作用,提示HR1LS/CF501免疫可诱导小鼠产生针对SARS-CoV-2和其他HCoVs的交叉中和抗体反应。
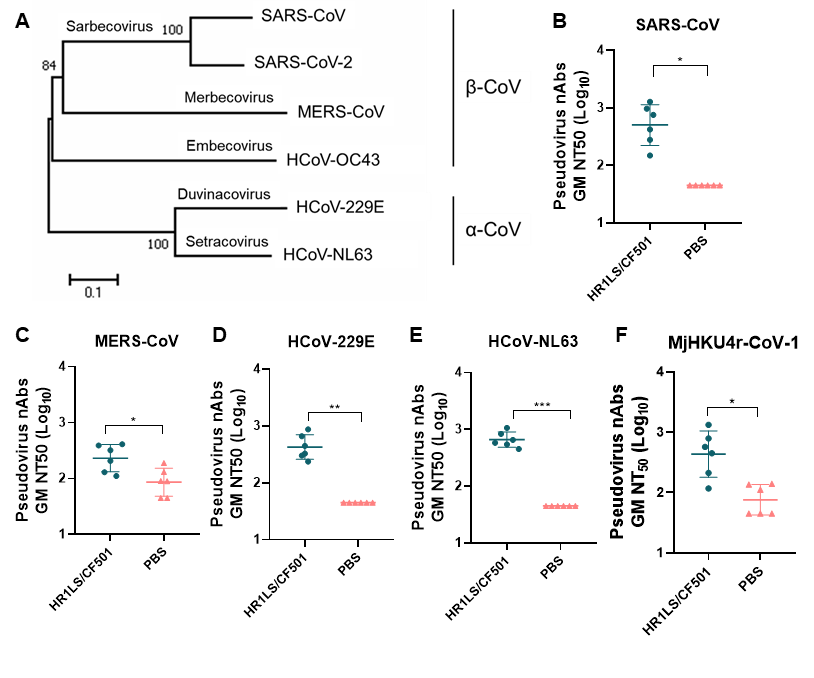
图6. 免疫小鼠血清对人和蝙蝠冠状病毒感染的中和活性
总之,该研究说明重组蛋白HR1LS既具有广谱抑制冠状病毒感染的能力,又可作为免疫原联合佐剂免疫诱导小鼠产生广谱抗冠状病毒抗体,具有进一步开发为广谱抗人冠状病毒入侵抑制剂或广谱冠状病毒疫苗的潜力。
去年11月,郑永唐/欧阳松应/姜世勃合作团队根据新冠病毒原始毒株S2亚单位中HR1和HR2序列设计和表达的HR121蛋白在免疫动物体内诱生的中和抗体可有效中和新冠病毒原始毒株和主要变异株(VOC)及奥米克戎亚谱系的感染,可开发成一种广谱抗新冠病毒及其变异株疫苗,而HR121蛋白也可有效地抑制新冠病毒原始毒株及其变异株和奥米克戎亚谱系的感染(https://doi.org/10.1016/j.apsb.2023.05.030)。
综合以上发现,姜世勃认为可以采用“以不变应万变”的策略,根据新冠病毒原始株S蛋白S2亚单位中保守位点来设计广谱抗冠状病毒疫苗和药物,用来防控现在和未来的新冠病毒变异株及将来新发与再现SARS样传染病的流行。
复旦大学博士后王欣玲和硕士生孙禄加为第一作者,上海市重大传染病和生物安全研究院双聘PI、复旦大学姜世勃教授,上海市重大传染病和生物安全研究院双聘PI、复旦大学陆路研究员和复旦大学王欣玲博士为共同通讯作者。感谢武汉病毒所周鹏研究员提供MjHKU4r-CoV-1包膜质粒。本研究得到国家重点研发计划、国家自然科学基金、上海市科技重大专项和上海市“科技创新行动计划”优秀学术/技术带头人项目的支持。
原文链接:https://doi.org/10.1080/22221751.2023.2244084

