近日,印度西孟加拉邦暴发尼帕病毒疫情,周边国家均提高警惕,一些国家(如泰国和尼泊尔)已相继加强针对来自印度旅客的卫生筛查措施,再次凸显了这一高致死性人畜共患病毒的严重威胁(https://www.thepaper.cn/newsDetail_forward_32464145)。尼帕病毒感染死亡率高达40%-75%,且目前全球尚无获批的特效药物,只有一个抗尼帕病毒抗体—m102.4已经完成一期临床试验(PMID: 32027842),所以临床应对手段极为有限。在此背景下,新型抗病毒药物的研发尤为迫切。
2026年1月12日,上海市重大传染病和生物安全研究院/复旦大学基础医学院教育部/卫健委/中国医科院医学分子病毒学重点实验室的姜世勃/陆路/王茜团队在新发突发病毒学领域的Top期刊(中科院1区)Emerging Microbes & Infections上发表了一篇题为“A highly potent, stable, and safe dePEGylated lipopeptide against Nipah virus and related henipaviruses”的研究论文。该研究成功设计并优化出一种去PEG化脂肽融合抑制剂VQ-P1-EK3-C16,在体外和体内均表现出对尼帕病毒(NiV)及其相关的亨德拉病毒(HeV)展现出皮摩尔(pM)级别超强的抑制活性、卓越的稳定性与广谱性,为应对此类高威胁病原体提供了极具前景的新型候选治疗策略。

尼帕病毒是一种可引发致命性脑炎的人畜共患病毒,被世界卫生组织列为优先疾病。研究团队针对病毒融合蛋白F的关键作用机制,通过自主设计的HR2 C端片段(HR2-CF)置换策略,成功去除传统脂肽抑制剂中的PEG链,避免了在健康人群体内广泛存在的抗PEG抗体所引起的免疫原性风险。进一步引入带电荷氨基酸突变(E/K),显著增强了肽链的螺旋稳定性与溶解性。
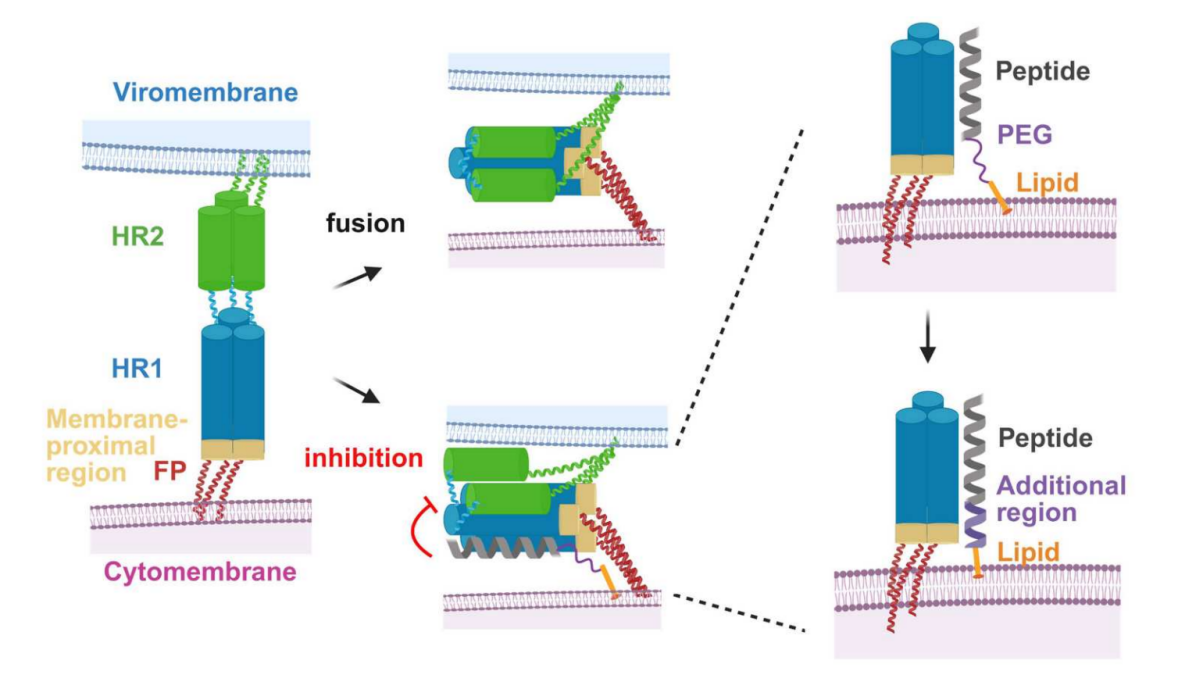
优化获得的脂肽VQ-P1-EK3-C16在体外实验中表现卓越。其对尼帕病毒马来西亚株(NiV-M)假病毒感染的半数抑制浓度(IC50)达0.48 pM,对尼帕病毒孟加拉株(NiV-B)和亨德拉病毒(HeV)同样高效,显示出广谱抗亨尼帕病毒活性。值得关注的是,其体外抗病毒活性相较于目前已完成I期临床试验抗NiV抗体m102.4的抗尼帕病毒活性 (IC50=0.27 nM,PMID: 18271743)强562。
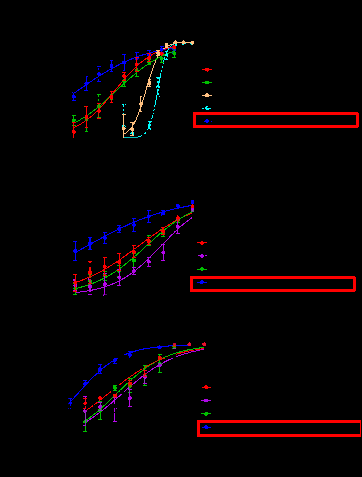
图2 去PEG化脂肽对NiV-M的抑制活性
在新生小鼠感染模型中,该脂肽能有效抑制NiV-M假病毒肺部与脑部感染,并显示出跨血脑屏障的能力,提示其对病毒性脑炎具有治疗潜力。机制研究表明,该脂肽能以高亲和力与NiV-HR1结合,阻断6-HB的形成。
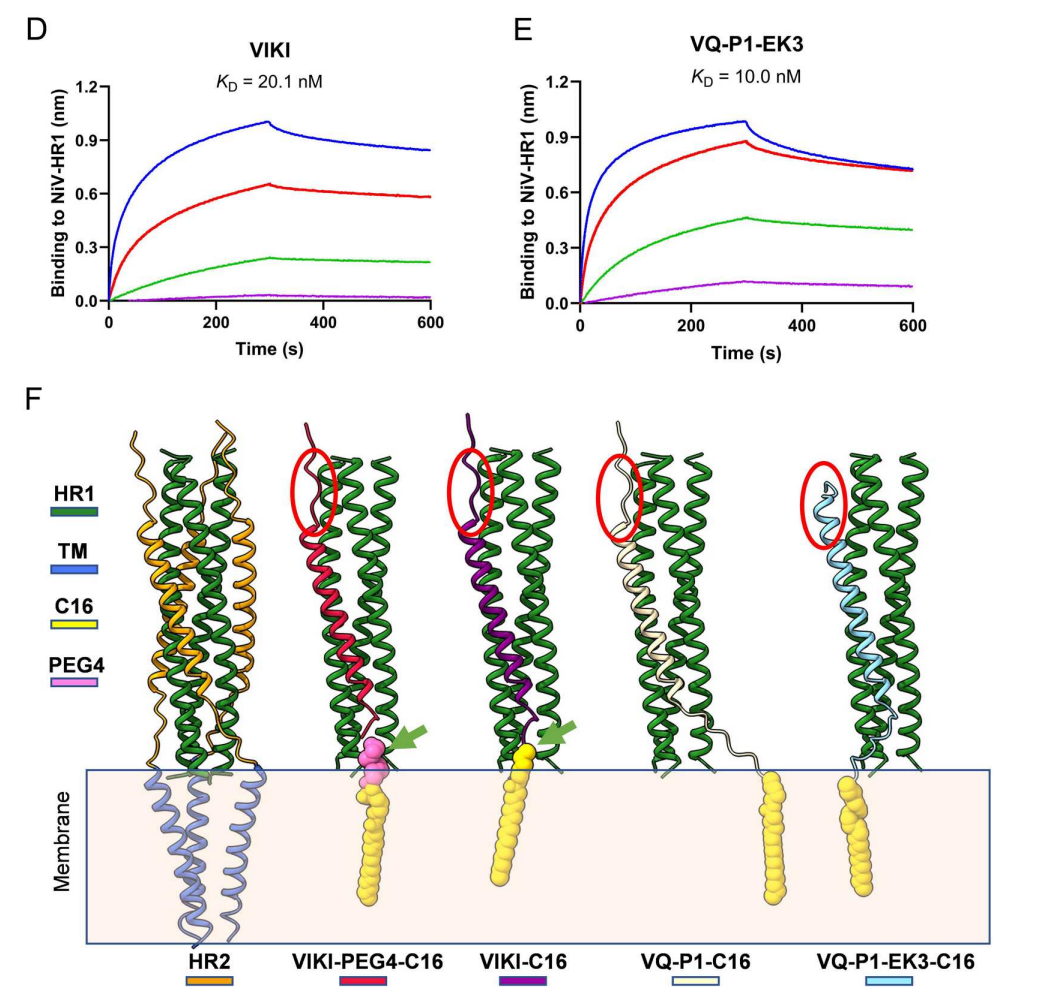
图3 VQ-P1-EK3-C16插入细胞膜与NiV-HR1结合
此外,VQ-P1-EK3-C16展现出优异的成药特性:在37℃储存90天后活性仅轻微下降;对蛋白酶降解具有强抵抗力;在动物体内血清半衰期近6小时,且静脉注射24小时后血药浓度仍维持超高抑制水平;细胞毒性低,选择(或治疗)指数(SI)超高。
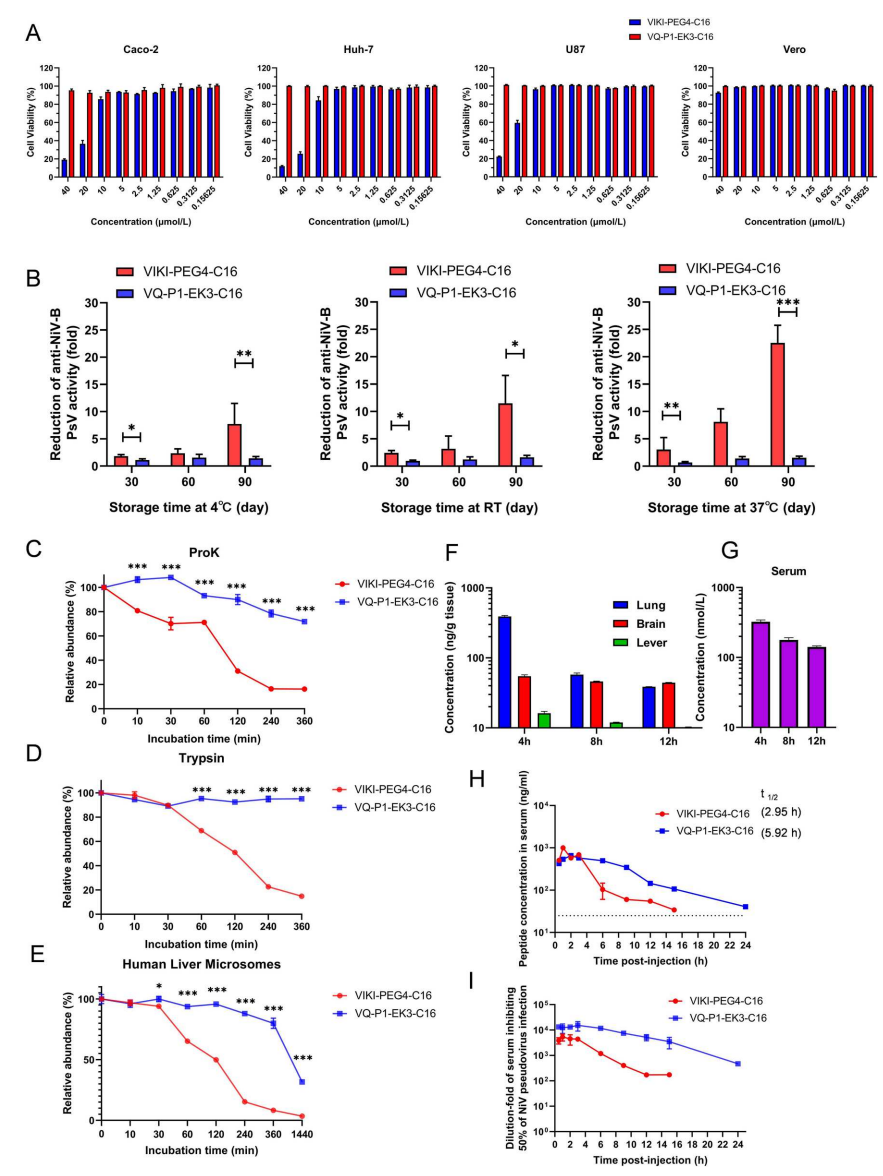
图4 VQ-P1-EK3-C16显示良好的成药性。
该研究成功开发出一种活性更强、稳定性更高且规避了抗PEG抗体反应相关风险的新型病毒融合抑制剂。在当前尼帕病毒疫情再现的背景下,此项工作不仅为未来应急治疗和药物储备提供了新的重要候选,也为针对其他包膜病毒的抑制剂设计提供了新思路。
上海市重大传染病和生物安全研究院/复旦大学基础医学院的姜世勃教授、陆路教授和王茜高级实验师为本文的共同通讯作者,王远舟博士研究生、王聪博士和周洁博士为共同第一作者。本研究由国家自然科学基金、上海市自然科学基金等多项基金支持。
原文链接:https://www.tandfonline.com/doi/full/10.1080/22221751.2025.2610858

